⼼臓の基本構造
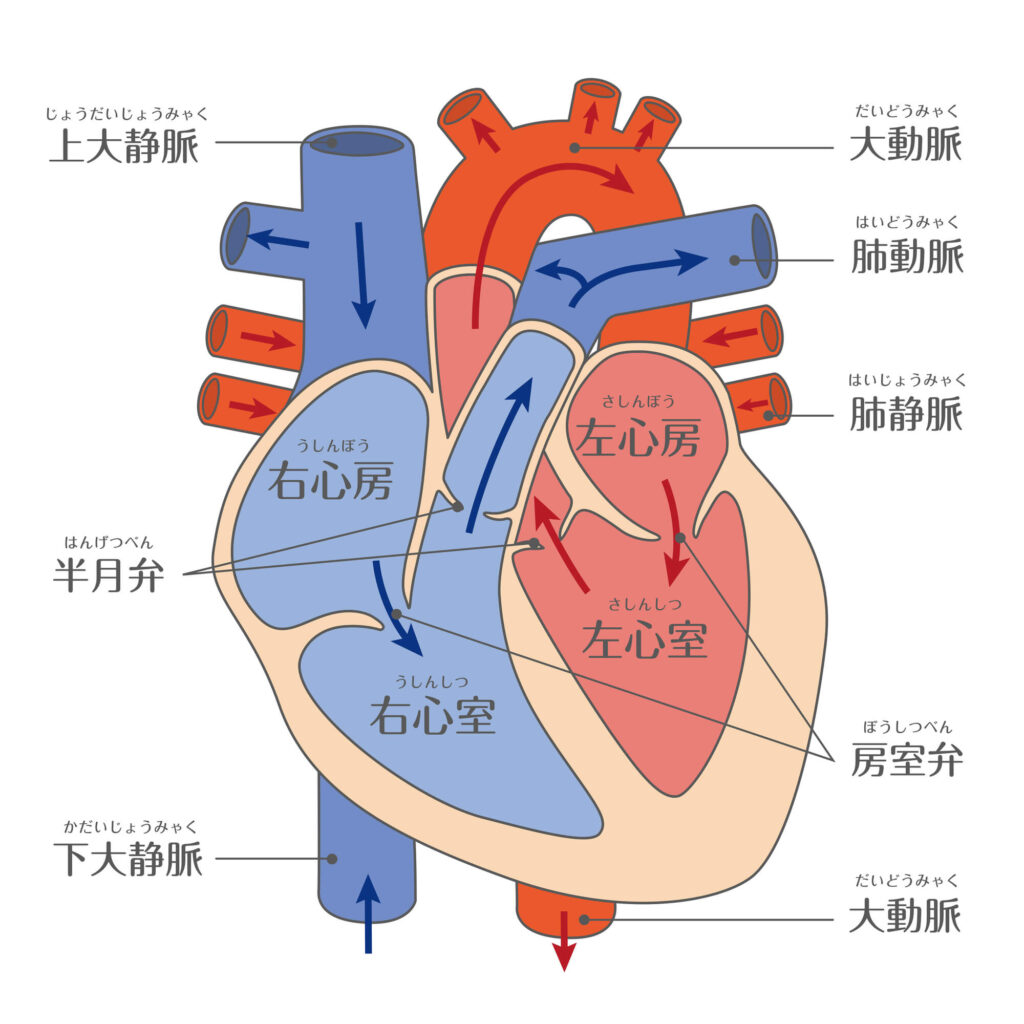
⼼臓は4つの部屋(左右⼼房、左右⼼室)に分かれています。⼼臓のポンプとしての役割は、主に⼼室が⾏っています。⼼房には全⾝ないし肺から⾎液が戻ってくるための⾎管(⼤静脈、肺静脈)がつながり、⼼室には全⾝ないし肺に⾎液を送り出すための⾎管(⼤動脈、肺動脈)がつながっています。
左右それぞれの⼼房と⼼室の間には、⾎液が、⼼房から⼼室⽅向に流れるように逆流防⽌弁があり、それぞれ三尖弁、僧帽弁と呼びます。
また⼼室から全⾝や肺に流れた⾎液が⼼臓に戻らない様に逆流防⽌弁があり、それを⼤動脈弁、肺動脈弁と呼びます。
また左右の⼼房⼼室の間には、酸素の少ない⾎液と多い⾎液が混ざらないように壁があり、それをそれぞれ⼼房中隔、⼼室中隔と呼びます。
先天性心疾患とは
先天性⼼疾患(Congenital heart disease, CHD)は⽣まれつき⼼臓や⾎管に通常と異なる構造となる疾患群です。遺伝⼦異常や環境要因などの影響を受けて、胎⽣50⽇頃までの⼼臓発⽣過程 に正常からの逸脱があって⽣じます。
出⽣数100⼈に1⼈程度で⾒られます。
成⼈先天性⼼疾患について
現在では、先天性⼼疾患を持って⽣まれた⽅の90%以上は成⼈となります。
15歳あるいは18歳以上の治療後・未治療を問わず先天性心疾患を有する「成⼈先天性⼼疾患(Adult congenital heart disease, ACHD)」の患者数は2007年に40万⼈を超え、2020年には50万⼈に達し、2023年には60万⼈を越えようとしています。
一方で、ACHDを専⾨に診る施設は少なく、⼩児病院などに通院していた⽅が、成⼈となって通院を⽌めてしまうケースがあります。⼗分な経過観察や診療を受けられずに重症化してしまうことが懸念され、スムーズな移⾏医療体制整備が望まれます。
先天性心疾患の⽀援・サポート
⾃⽴⽀援医療(育成医療)、⼩児慢性特定疾患に対する医療費助成、⾃⽴⽀援医療(更⽣医療)、難病に対する医療費給付など様々な公的助成制度があります。
⽇本⼩児循環器学会「⼀般の⽅へ」
https://www.heart-manabu.jp/
⼩児慢性特定疾病情報センター
https://www.shouman.jp/
難病情報センター
https://www.nanbyou.or.jp/
全国⼼臓病の⼦どもを守る会
https://www.heart-mamoru.jp/index.html
先天性⼼疾患情報ポータル
https://j-achd.jp/
⽇本⼼臓財団 ⼦どもの⼼臓病について
https://www.jhf.or.jp/check/child/
先天性⼼疾患の分類

- ⼆⼼室型:体⼼室・肺⼼室とも⼗分に機能し、⼆⼼室修復を⽬指す
- 単⼼室型:⼀⼼室機能しかなく、単⼼室修復(最終的にフォンタン⼿術)を⽬指す
- 不定型:上記いずれか定まらないもの
⽣後の治療過程の⼤筋を決定づける上記の分類から病態をとらえていきます。
単⼼室では、体⾎流と肺⾎流の両⽅が1つの⼼室から駆出されており、正常の左⼼室よりも単⼼室にかかる容量の負荷は⼤きくなります。
初回は肺動脈絞扼⼿術や体肺動脈短絡⼿術によって肺⾎流と体⾎流のバランスをとり、次にグレン(Glenn)⼿術により上半⾝の静脈⾎を⼼臓を介さずに肺に流し、下半⾝の静脈⾎は⼼臓を通って酸素化された肺静脈⾎と混合されて体に流れるようになります。
Glenn⼿術後は単⼼室は体⾎流量を送りだせば良くなるため、容量の負荷はだいぶ軽減されますが、右左短絡が残りチアノーゼが続きます。
最終的にはフォンタン(Fontan)⼿術を⾏い、下半⾝の静脈⾎も⼼臓を介さずに肺に流れるようになり、理想的にはチアノーゼも解消されます。実際には、⼼臓の静脈⾎や肺内の動静脈短絡など右左短絡が残りチアノーゼとなることもあります。
また⻑期的には肺に⾎液を送る⼼室(ポンプ機能)がないため、内臓臓器に負荷が継続してかかる状態となり、Fontan術後遠隔期に、不整脈、チアノーゼ、⾎栓塞栓症、蛋⽩漏出性胃腸症、⼼不全、肺⾼⾎圧、肝硬変、肝がん、腎不全など全⾝の臓器不全をきたすフォンタン術後症候群となることもあります。
そのため可能な限り2⼼室もしくは1.5⼼室(Glenn⼿術追加により、肺⼼室への容量負荷軽減)を⽬指します。
⼀⽅で、条件の良いFontan循環では、super Fontanと呼ばれる健常⼈と遜⾊ない運動耐容能を持つ⽅もいて、必ずしもFontan循環が良くないとも⾔えず、いずれのpathwayを選択するかが難しい⽅もいます。
他にも、下記のような分類もなされます。
- 肺⾎流増加型/肺⾎流減少型
(肺⾎流量が増加ないし減少する先天性⼼疾患の分類) - チアノーゼ性⼼疾患/⾮チアノーゼ性⼼疾患
(チアノーゼとは酸素供給の減少・⾎液中の酸素飽和度の低下により、⽪膚や粘膜が⻘ 紫⾊に⾒える状態であり、チアノーゼとなりやすいか酸素供給に影響がないかで区分する分類) - 左右短絡疾患/右左短絡疾患
(肺で酸素化された⾎液が流れる左⼼系(体循環)と体から返ってくる⾮酸素化⾎が流れる右⼼系(肺循環)に短絡(シャント)があり、左→右ないし右→左いずれかが優位となりやすい先天性⼼疾患の分類) - 単純性⼼疾患/複雑性⼼疾患
先天性⼼疾患の症状
1.肺⾎流増加により⾒られる症状
新⽣児期・乳児期:多呼吸、陥没呼吸、呼吸困難、喘鳴、多汗、哺乳障害幼児期:多呼吸、易感染性、反復する肺炎
⼩児期:運動能低下、息切れ
2.肺⾎流減少により⾒られる症状
新⽣児期・乳児期:チアノーゼ
幼児期:チアノーゼ、低酸素発作、蹲踞(しゃがみ込み)
⼩児期:チアノーゼ、ばち状指
3.低⼼拍出量により⾒られる症状
新⽣児期・乳児期:蒼⽩、末梢冷感、冷や汗、網状チアノーゼ、体重増加不良、弱い鳴き声幼児期:体重増加不良、運動発達遅延、易疲労性、顔⾊不良、やせ
⼩児期:運動能低下、動悸
4.思春期以降に合併する症状
胸痛、失神発作、突然死、喀⾎、不整脈、出⾎傾向、痛⾵、けいれん など
背景となる先天性⼼疾患の病態により、症状の別や強弱は様々です。上記の症状が⾒られたからといって必ずしも先天性⼼疾患によるものとは限りません。
代表的な先天性⼼疾患

1.⼼室中隔⽋損症 ventricular septal defect (VSD)
https://www.shouman.jp/disease/details/04_45_057/
出⽣1000⼈に1~4⼈、先天性⼼疾患の20-30%にみられ最多の疾患です。
左右の⼼室を隔てる中隔壁が完全には形成されず⽋損孔が残ったものです。先天性⼼疾患の中で最多の疾患です。
⽋損孔の⼤きさにより無症状から⼼不全まで病態に幅があります。⼼室中隔⽋損を通して、酸素化された左⼼室の⾎液が右⼼室を通って肺に流れやすく、肺⾎流量が増加します(左右短絡)。全⾝に必要な⾎流に加えて、⼼臓と肺を循環する⾎流量が増えて⼼臓に対する容量の負荷となりますが、⼼臓が⼗分な⾎液量を送り出せなくなると、体に必要な⾎液量が相対的に減少して⼼不全症状を伴ってきます。また肺⾎流の増加や肺⾎管にかかる⾎圧の上昇により、肺⾼⾎圧症となることがあります。
肺⾼⾎圧が進⾏すると右室圧が左室圧を超えて、⼼室中隔⽋損孔を通して酸素化されていない右室の⾎液が左室を通って体に送られ(右左短絡)、肺⾎流は減少し、チアノーゼ・低酸素⾎症となる病態(アイゼンメージャ症候群)となります。アイゼンメージャー症候群では⼿術治療困難であり⽣命予後も不良となることが知られています。
⼼不全を伴う⼤⽋損やアイゼンメージャー症候群への進⾏悪化が予測される場合に⼼室中隔⽋損症⼿術(⽋損孔の閉鎖)の適応となります。近年では⼩児期にアイゼンメージャー症候群として⼿術を受けられなかった成⼈の⽅が、肺⾼⾎圧治療薬を導⼊して肺⾼⾎圧の改善を得てから⼿術(treat & repair)を⾏うこともあります。
症状としては疲れやすい、ミルク哺乳不良、体重増加不良、頻呼吸・息切れ、頻脈・不整脈などがあります。無症状で⽋損孔も⼩さければ経過観察されることもありますが、⼩⽋損でも⼼室中隔⽋損に近接する⼤動脈弁に変形をきたす(ベンチュリー効果 : Venturi effectによる弁尖の変形や穿孔を⽣じ、弁逆流を伴うなど)など弁疾患を合併する場合にも⼿術適応となります。
⼿術は、⼈⼯⼼肺下、⼼停⽌下に⽋損孔をパッチ閉鎖(EPTFEや⾃⼰⼼膜など)もしくは⼩⽋損の場合に直接閉鎖します。
2.⼼房中隔⽋損症 atrial septal defect (ASD)
2次孔型
https://www.shouman.jp/disease/details/04_43_053/
静脈洞型
https://www.shouman.jp/disease/details/04_43_054/
1000⼈に1~2⼈、先天性⼼疾患の10-15%にみられます。
左右の⼼房を隔てる⼼房中隔に⽋損のある状態です。発⽣過程において、左右の⼼房に始めからある1次孔をふさぐように1次中隔壁が形成され、⼼室側の房室中隔と接合し1次孔が閉鎖しますが、1次孔が閉鎖される頃には、1次中隔に退縮がみられ新たな⽋損孔、2 次孔ができます。
この2次孔をふさぐ様に2次中隔が形成され、1次と2次の中隔が重なり合って1次中隔がフラップ状となり胎児循環に必要な右左交通が残ります。出⽣後には⽣理的に肺⾎流が増加し、左房圧が上昇して両中隔が癒合して中隔壁が完成します。癒合せずにフラップ状の交通が残る場合は卵円孔開存と称し、明らかな⽋損孔が⾒えるものは⼼房中隔⽋損症です。短絡⾎流の多い場合は、⼼不全や肺⾼⾎圧のリスクがあり治療適応となります。
1次孔が残存する場合、⼼房中隔のみならず房室中隔の異常と考えられ、房室中隔⽋損症に分類されます。⼼房に流⼊する、上下⼤静脈や肺静脈、冠状静脈(⼼臓の静脈)の接続部に⽋損孔(左右⼼房間交通)が残存する場合も静脈洞型の⼼房中隔⽋損症に分類されます。いずれにせよ、⼼不全や肺⾼⾎圧リスクなどにより⼿術適応を決定します。
⼿術は⼈⼯⼼肺下、⼼停⽌下に直接閉鎖またはパッチ閉鎖(⾃⼰⼼膜やEPTFE)します。
3.動脈管開存症 patent ductus arteriosus (PDA)
https://www.shouman.jp/disease/details/04_42_051/
1000⼈に0.2~0.5⼈、先天性⼼疾患の5%以下にみられます。
⼤動脈と肺動脈をつなぐ動脈管は胎児期には必要な⾎管です。呼吸をしていない胎児の肺は肺⾎管抵抗が⾼くあまり⾎液を必要としていません。右室から肺動脈に流れた⾎液は動脈管を介して⼤動脈に流れ、全⾝に⺟体・胎盤由来の酸素や栄養を供給しています。
出⽣後には呼吸を始めて肺が拡張し肺⾎管抵抗が低下します。肺動脈から⼤動脈に向けて流れていた動脈管の⾎流も、⾎管抵抗の変化により⼤動脈から肺動脈に向けて流れる様になります。動脈管を流れる⾎液の酸素飽和度が上昇することや、胎盤由来の動脈管拡張因⼦(プロスタグランジン)が失われることで動脈管は狭⼩化・閉鎖していきます。満期産児の90%以上は⽣後4⽇以内に⾃然閉鎖します。
閉鎖せずに残ったものが動脈管開存症となります。短絡⾎流の多い場合は、⼼不全や肺⾼⾎圧のリスクがあり早期の⼿術適応となります。短絡量が少なくても、感染性⼼内膜炎などのリスクからカテーテル治療等を⾏うこともあります。
⼿術は動脈管の⾎管クリップ閉鎖や結紮を⾏います。
4.ファロー四徴症 tetralogy of Fallot (TOF)
https://www.shouman.jp/disease/details/04_33_041/
https://www.nanbyou.or.jp/entry/4741
1000⼈に0.3~0.9⼈、先天性⼼疾患の5%以下にみられます。チアノーゼ性⼼疾患の中では最多(約30%)の疾患です。
ファローの4徴とは、⼤動脈騎乗、⼼室中隔⽋損、肺動脈狭窄・右室流出路狭窄、右室肥⼤を指します。1888年にフランス⼈のFallot により、当時blue babyと呼ばれていたチアノーゼを呈する児の中に上記の4つの特徴をもつ⼼疾患が提唱されたことからファロー四徴症と呼ばれています。
⼼臓発⽣過程において1本の筒状の原始⼼筒から両⼼室・⼼房、⼤⾎管が形成されますが、両⼼室の⼼尖側と⼤⾎管を含めた流出路の接合がうまく整列しなかったために流出路の⼼室中隔が、⼼尖部側の中隔に対し右前⽅に偏位してしまいます。中隔壁の不整合から⼼室中隔⽋損、肺動脈狭窄・右室流出路狭窄を⽣じ、右室圧は左室圧とほぼ等圧になります。⾼い圧にさらされて右室肥⼤となります。
少ない肺⾎流・チアノーゼを改善するために、プロスタグランジン 製剤を⽤いて動脈管を開存させたり、体肺動脈短絡⼿術(Blalock-Thomas-Taussigシャント)など⼈⼯⼼肺を⽤いない姑息⼿術、⼈⼯⼼肺を⽤いた⼼内修復⼿術が⾏われます。Pink Fallotと呼ばれるチアノーゼを呈さないものから、肺動脈閉鎖を伴う極型Fallotまで、病態もさまざまであり、治療⽅針は姑息⼿術を先⾏するなど個々に判断されます。
⼼内修復⼿術では、⼼室中隔⽋損のパッチ閉鎖、右室流出路の筋性狭窄解除、肺動脈弁・肺動脈狭窄解除など複合的な⼿術操作となります。⾃⼰弁の温存の可否、遺残する右室流出路・肺動脈狭窄や肺動脈弁逆流など遠隔期に再介⼊を要することもあり、⼿術後も定期的な病態のチェックが必要となります。
その他の複雑性先天性⼼疾患
房室中隔⽋損症 atrioventricular septal defect (AVSD)
完全型
https://www.shouman.jp/disease/details/04_44_056/
不完全型
https://www.shouman.jp/disease/details/04_43_055/
肺動脈閉鎖症 pulmonary atresia (PA) 純型肺動脈閉鎖 (PA-IVS)
https://www.shouman.jp/disease/details/04_32_040/
https://www.nanbyou.or.jp/entry/4483
⼼室中隔⽋損を伴う肺動脈閉鎖 (PA-VSD)
https://www.shouman.jp/disease/details/04_32_039/
https://www.nanbyou.or.jp/entry/4876
三尖弁閉鎖症 tricuspid atresia (TA)
https://www.shouman.jp/disease/details/04_31_038/
https://www.nanbyou.or.jp/entry/4480
Ebstein奇形 Ebstein’s anomaly
https://www.shouman.jp/disease/details/04_38_047/
https://www.nanbyou.or.jp/entry/4486
完全⼤⾎管転位症 transposition of the great arteries (TGA)
https://www.shouman.jp/disease/details/04_36_045/
https://www.nanbyou.or.jp/entry/4477
修正⼤⾎管転位症 congenitally corrected TGA (cTGAないしccTGA)
https://www.shouman.jp/disease/details/04_37_046/
https://www.nanbyou.or.jp/entry/4474
両⼤⾎管右室起始症 double outlet right ventricle (DORV)
https://www.shouman.jp/disease/details/04_34_043/
https://www.shouman.jp/disease/details/04_34_042/
https://www.nanbyou.or.jp/entry/4873
⼤動脈縮窄症・縮窄複合 coarctation of aorta (CoA)・complex CoA
https://www.shouman.jp/disease/details/04_56_070/
https://www.shouman.jp/disease/details/04_56_071/
⼤動脈離断症・離断複合 interruption of aortic arch (IAA)・complex IAA
https://www.shouman.jp/disease/details/04_57_076
https://www.shouman.jp/disease/details/04_57_075/
総肺静脈還流異常症 total anomalous pulmonary venous connection (TAPVC)
https://www.shouman.jp/disease/details/04_46_058/
部分肺静脈還流異常症 partial anomalous pulmonary venous connection (PAPVC)
https://www.shouman.jp/disease/details/04_46_059/
単⼼房 single atrium (SA)
https://www.shouman.jp/disease/details/04_43_052/
単⼼室 single ventricle (SV)
https://www.shouman.jp/disease/details/04_30_037/
https://www.nanbyou.or.jp/entry/4369
総動脈幹遺残症 persistent truncus arteriosus (PTA)
https://www.shouman.jp/disease/details/04_39_048/
https://www.nanbyou.or.jp/entry/4895
左⼼低形成症候群 hypoplastic left heart syndrome (HLHS)
https://www.shouman.jp/disease/details/04_29_036/
https://www.nanbyou.or.jp/entry/4372
内臓錯位症候群 heterotaxy syndrome 無脾症/右側相同 asplenia/right isomerism
https://www.shouman.jp/disease/details/04_65_096/
多脾症/左側相同 polysplenia/left isomerism
https://www.shouman.jp/disease/details/04_65_097/
先天性⼼疾患⼿術に関連する合併症や遠隔期の問題

⼼不全・低⼼拍出量症候群(low output syndrome, LOS)
⼼臓は⾃⾝の⾎管、冠動脈に⾎液が流れて拍動しているのが最も⽣理的です。⼿術中の⼈⼯⼼肺や⼼停⽌によって、⼼臓のポンプ機能は術前よりは低下します。全⾝に⼗分な⾎液が送れなくなった状態が⼼不全・LOSです。
多かれ少なかれ、術後の⼼機能低下は想定されるため、⼼機能回復を待つ間は、強⼼薬や⾎管拡張薬を⽤いて循環のサポートをします。2⼼室修復やFontan修復を終えていない、姑息⼿術後などでは、体と肺に流れる⾎流量のバランスをとるためにより複雑な周術期管理が⾏われます。
薬だけでは⼼臓の機能が保てない時には、機械的な補助循環装置を必要とすることもあります。補助循環使⽤中は、⾎液が固まらないようにヘパリンという薬剤を使⽤して⾎液が固まらない状態にして管理することになります。そのため出⾎の危険性が通常よりも⾼まります。
また、ヘパリンを使⽤しているにもかかわらず⾎栓(⾎の塊)を形成する可能性があり、これらが全⾝に⾶んでしまい、各臓器に⾎栓閉塞による梗塞(臓器への⾎液灌流が阻害され臓器障害を⽣じる)、循環不全に伴う虚⾎性病変(特に腸管、⼿⾜など末梢の虚⾎)が出現する可能性もあります。
⼼タンポナーデ
⼿術終了時に完全に⽌⾎する事は出来ません。そのため⼼臓の周りにドレーンという管を⼊れ、⾎液が⼼臓の周りに溜まらないようにします。
もしこのドレーンが詰まったら、⼼臓の周りに⾎液が溜まり、⼼臓を圧迫し、⼼臓の機能を悪くします。そのため低⼼拍出量症候群となると⼼タンポナーデと呼び、緊急⼿術で溜まった⾎液を取り出す必要があります。
また、この⼼タンポナーデは、術後急性期には主に出⾎が原因ですが、術後しばらく経ってから(ときに退院後も)、⼼嚢⽔と呼ばれる⼼臓の周囲に溜まる体液成分によっても起こる可能性があります。この場合も、緊急でもう⼀度胸を開けたり、針で穿刺して貯留液を除去したり、ドレーンを再留置したりする必要があります。
不整脈
脈が早くなる頻脈性と遅くなる徐脈性の不整脈があります。頻脈の際は鎮静、体温管理や薬剤にて、徐脈の場合は体外式のペースメーカーによる電気的な刺激で脈拍をコントロールします。
問題となるのは、コントロールが間に合わずに低⼼拍出量症候群となり⼼臓⾃⾝も低還流にてより⼼機能を落として負のスパイラルに陥る場合です。その際は⾎圧が低下し(ショック)、蘇⽣や補助循環を必要とすることもあります。
また房室ブロックと呼ばれる徐脈性の不整脈は術後回復しない場合に体内にペースメーカーを植え込む追加⼿術を必要とすることがあります。
⾎栓塞栓症・冠動脈関連の合併症
⼼停⽌を伴う⼿術では、⼀般に⼼筋保護液で⼼筋を還流して⼀時的な⼼筋の虚⾎による障害を防ぎます。⼼筋保護液は⼼筋の⾃動的な収縮活動を停⽌させることで、酸素消費量をおよそ10分の1に減らし、虚⾎に耐える時間を延⻑させています。
⼼臓の栄養⾎管である冠動脈には、時に⼼室内や⼼静脈への交通があるなど、局所的に不⼗分な⼼筋保護液還流となる可能性があります。その結果、致死的な不整脈や⼼機能の低下をきたす可能性がります。
開⼼術では⼼内に空気が⼊ってしまいます。⾎流再開前にその空気を除去しますが、残存する微⼩な気泡が⼩⾎管に流れて詰まらせてしまう(空気塞栓)ことがあります。冠動脈に空気塞栓を⽣じた場合に術中に⼀時的に不整脈や⼼電図変化が出現したりしますが、多くは⾎流再開して回復します。
また、⼈⼯⼼肺中は回路内で⾎栓が⽣じやすく、⾎液凝固を阻害するヘパリンを投与していますが、それでも⾎栓ができてしまい⾎栓塞栓症を合併することが考えられます。冠動脈が詰まると⼼筋梗塞となり、脳⾎管に詰まると脳梗塞を合併することとなります。また脳梗塞に続いて脳出⾎を伴うこともあり、いずれも致命的となりうる合併症です。
いずれも頻度の低い合併症ですが、起きてしまうと重⼤な合併症となります。
肺⾼⾎圧症・肺⾼⾎圧緊急(Pulmonary Hypertensive crisis)
左右短絡疾患など肺⾼⾎圧症を合併している場合に、⼿術後に肺⾼⾎圧の急速な進⾏悪化が⾒られ、肺⾎流が流れにくくなる発作を肺⾼⾎圧緊急と呼びます。特に2⼼室修復術後では、右⼼から⾎液が流れ出なくなり、左⼼に帰ってくる⾎流がなくなり左室は充満することなく⾎液を駆出できなくなり、低⼼拍出量症候群や低酸素⾎症となり急変し救命困難となることがあります。
術前に肺⾼⾎圧の合併を認める場合は、肺⾎管拡張薬など予防投与を⾏い発作を起こさせない管理が重要です。
呼吸器合併症
⼿術後の出⾎が⼼臓まわりに溜まると⼼タンポナーデとなりますが、⼼嚢と胸腔に交通があったり、術中の肺損傷から出⾎するなど胸腔に⾎液が貯留することがあり、この状態を⾎胸と⾔います。
普段私たちは空気を吸い込んで陰圧呼吸を⾏っています。⼿術中は、⼈⼯呼吸器により気管まで⼊れた管を通して肺に圧がかかる陽圧呼吸となっています。この圧により肺が破れる事があり、この状態を気胸と呼びます。
術前に気道系に細菌を保持している場合は、肺が破れた際に細菌が胸腔や⼼嚢内に出てしまうことになり、膿胸や、縦隔洞炎といった重症感染症を引き起こす可能性があります。また、術後肺へ流れる⾎液の量が増加したり、上半⾝の静脈圧が上昇することにより胸に⽔がたまる事があり、これを胸⽔と呼びます。ときにこの胸⽔は、体の中の脂肪成分を含んで⽩濁の胸⽔となることがあります。
この場合は乳び胸といいます。⾎胸、気胸、胸⽔、乳び胸の治療には、胸に管(ドレーン)を留置する処置が必要となったり、肺と胸壁を癒着させたりすることで胸⽔の溜まるスペースをなくし、胸⽔の流出を⾷い⽌めるために特殊な薬剤を胸腔内に投与する場合もあります。
これらの処置を⾏う際には、針やドレーンを胸腔内に⼊れる際に肋⾻と肋⾻の間に⾛⾏する肋間動静脈や、胸壁の⾎管を損傷して2次的に⾎胸を起こし、緊急で対応しなくてはならない状況に陥ることもあります。またスポンジ状の肺からは、⼿術後たくさん痰が出ます。これをうまく出せなかったり、ヘパリン使⽤下で肺や気管、気管⽀から出⾎し、これらが気道に詰まったりすることで、肺まで空気が⼊らなくなり無気肺となることがあります。このような場所で細菌感染をおこすと肺炎になります。
神経合併症
横隔神経⿇痺
横隔膜は、息を吸うと下がり、吐くと上がるという呼吸の補助をしますが、神経が⿇痺すると横隔膜が動かなくなります。1側の横隔神経⿇痺では、対側の横隔膜や胸壁を⽤いて呼吸ができることがほとんどですが、腹圧と胸腔内圧では腹圧の⽅が⾼く、横隔膜が挙上して、胸腔の容積が⼩さくなり、呼吸の妨げとなることがあります。その場合は、横隔膜縫縮術により横隔膜を低い位置に引き下げる⼿術治療が有効となります。
反回神経⿇痺
反回神経が障害されると、声⾨周囲の動きが悪くなります。声がかすれる嗄声となったり、ものを飲み込む時に誤嚥してしまう事があります。この反回神経⿇痺は、⼿術操作だけでなく、⼈⼯呼吸器の管などが機械的に声⾨に接触することによっても起こりえますので、⻑期⼈⼯呼吸器管理を⾏う患者様の場合は反回神経⿇痺を合併する可能性があります。反回神経⿇痺の場合は経過観察することがほとんどですが、誤嚥の程度によって、経⼝摂取を中⽌し⿐から胃に管を⼊れて栄養を注⼊する必要があることもあります。
感染
縦隔洞炎
⼼臓が納まっているスペースを解剖学的に前縱隔洞と呼びます。⼼臓⼿術の術後に、この前縱隔洞内で感染を起こした状態を「前縱隔洞炎」と呼びます。前縱隔洞は⾎流が豊富な組織ではなくスペースであるため、抗⽣剤が届きくく、抗⽣剤投与だけでは難しく、再度創部を開けて、排膿した上、洗浄、ドレーン留置などが有効となります。
創部離開
⼿術の創が何らかの理由で開いてしまう状態ですが、感染に伴って離開することもあれば、無菌でも⾎流不全などが原因で創部の治癒が阻害されて離開することがあります。感染巣や虚⾎壊死組織の除去が必要で外科的な処置・⼿術が必要となります。
肝臓や腎臓など臓器機能障害
⼼臓、腎臓、肝臓はいずれもエネルギー需要の⼤きい臓器で細胞内にミトコンドリアが豊富に含まれています。ミトコンドリアは酸素が存在する条件下で効率的にエネルギーを酸性してくれます。
⼈⼯⼼肺⼿術中や⼼不全合併例など内臓臓器⾎流(酸素供給)が不⾜すると肝臓や腎臓などの主要臓器の機能が低下することがあります。ほとんどの場合は⼀過性の変化ですが、稀に⻑期化することがあります。
単⼼室型機能的根治術であるフォンタン⼿術後や、根治術は終了したものの、体静脈圧(全⾝の臓器から戻ってくる静脈の⾎液の圧)が⾼い状態にある⼆⼼室型根治術後には、⻑期にわたって⾼い体静脈圧に臓器がさらされる結果、遠隔期に肝機能障害、肝臓の繊維化、肝硬変様の変化を⽣じる場合があります。術後急性期に問題となることではありませんが、術後も定期的に肝臓の機能を経過観察していくことが必要になります。
遺残病変
⽋損孔閉鎖後のリーク(漏れ)、⾎管形成後の再狭窄、弁形成後の弁逆流、弁狭窄など。程度により再⼿術となることがあります。
成⻑に伴う再⼿術
⼿術の際に⼈⼯物(⼈⼯⾎管、⼈⼯弁、パッチなど)を使⽤せざるを得ないことがあります。⼈⼯物は成⻑しませんので、患児の成⻑に伴って相対的に⼩さくなってしまいます。そのためサイズアップ(再⼿術)を要することがあります。
輸⾎合併症
⼈⼯⼼肺⼿術では回路内に充填された液体で⾎液が希釈されてしまいます。そのため貧⾎となりますと、全⾝への酸素の運搬能が低下し、⾼度の貧⾎では特に脳への影響が懸念されます。
新⽣児期、乳児期早期の⼿術では、⼈⼯⼼肺回路充填量が体の⾎液量に対して多くなり、輸⾎なしでは⼿術そのものが困難になります。また、⼼不全の管理においても、輸⾎による貧⾎の是正は酸素供給を増やし有効となります。
輸⾎した場合にB型肝炎、C型肝炎、HIV(AIDS)感染などの輸⾎後感染症は数⼗万から数百万に1件と少なく、⼿術治療全体のリスクと⽐較し低くなっています。その他、細菌感染、輸⾎後肺障害、アレルギー・アナフィラキシーショックなどで重症化するのは万に1件程度となっています。
フォンタン(Fontan)術後症候群
https://www.shouman.jp/disease/details/04_66_098/
⽇本成⼈先天性⼼疾患学会 ⼀般の⽅へ
https://www.jsachd.org/public/
⼼疾患患者の妊娠・出産の適応,管理に関する ガイドライン(2018 年改訂版)
https://www.j-circ.or.jp/cms/wp-content/uploads/2020/02/JCS2018_akagi_ikeda.pdf
上記に、表 62 ⼼疾患をもつ患者さんとご家族のための,妊娠・出産に関する⼿引きがあります。
⼼臓病の⼈の妊娠・出産 | ⽇本⼩児循環器学会【⼀般の⽅へ】
https://www.heart-manabu.jp/gp
(2024年1⽉ 益澤明広)




